Produktnamme:Metyletylketon
Molekulêre opmaak:C4H8O
CAS-nûmer:78-93-3
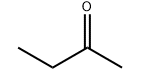
Produkt molekulêre struktuer:
Spesifikaasje:
| Ûnderdiel | Ienheid | Wearde |
| Suverens | % | 99.8 min |
| Kleur | APHA | 8max |
| Soere wearde (as asetaatsoer) | % | 0.002maks |
| focht | % | 0.03maks |
| Ferskining | - | Kleurleaze floeistof |
Gemyske eigenskippen:
Metyletylketon is gefoelich foar ferskate reaksjes fanwegen syn karbonylgroep en de aktive wetterstof neist de karbonylgroep. Kondensaasje fynt plak as it ferwaarme wurdt mei sâltsoer of natriumhydrokside om 3,4-dimethyl-3-hekseen-2-on of 3-methyl-3-hepteen-5-on te produsearjen. As it lange tiid oan sinneljocht bleatsteld wurdt, wurde etaan, jittiksoer en kondensaasjeprodukten produsearre. Genereart diacetyl as it oksidearre wurdt mei salpetersoer. As it oksidearre wurdt mei sterke oksidaasjemiddels lykas chromsoer, wurdt jittiksoer generearre. Butanon is relatyf stabyl foar waarmte, en termyske splitsing by hegere temperatueren produseart enon of methylenon. As it kondinsearre wurdt mei alifatyske of aromatyske aldehyden, wurde ketonen mei in heech molekulêr gewicht, sykliske ferbiningen, ketonkondensaasje en harsen produsearre. Bygelyks, kondensaasje mei formaldehyde yn 'e oanwêzigens fan natriumhydrokside produseart earst 2-methyl-1-butanol-3-on, folge troch dehydrataasje ta methacrylaton.
Harsfoarming fynt plak by bleatstelling oan sinneljocht of UV-ljocht. Kondensaasje mei fenol jout 2,2-bis(4-hydroxyfenyl)butaan. Reagearret mei alifatyske esters yn 'e oanwêzigens fan in basiske katalysator om β-diketonen te produsearjen. Asylaasje mei soer anhydride yn 'e oanwêzigens fan in soere katalysator om β-diketonen te foarmjen. Reagearret mei wetterstofcyanide om cyanohydrine te foarmjen. Reagearret mei ammoniak om ketopiperidinederivaten te foarmjen. It α-wetterstofatoom fan butanon wurdt maklik ferfongen troch halogenen om ferskate halogenearre ketonen te foarmjen, lykas 3-chloro-2-butanon troch ynteraksje mei chloor. Ynteraksje mei 2,4-dinitrofenylhydrazine produseart giele 2,4-dinitrofenylhydrazon.
Oanfraach:
Metyletylketon (2-butanon, etylmetylketon, metylaceton) is in organysk oplosmiddel mei relatyf lege toksisiteit, dat yn in protte tapassingen fûn wurdt. It wurdt brûkt yn yndustriële en kommersjele produkten as oplosmiddel foar lijmen, ferve en skjinmaakmiddels en as ûntwaaksoplosmiddel. Metyletylketon, in natuerlik ûnderdiel fan guon iten, kin troch fulkanen en boskbrannen yn it miljeu frijkomme. It wurdt brûkt by de produksje fan reekleaze poeier en kleurleaze keunstharsen, as oplosmiddel en yn oerflakcoatings. It wurdt ek brûkt as smaakstof yn iten.
MEK wurdt brûkt as oplosmiddel foar ferskate coatingsystemen, bygelyks vinyl, kleefstoffen, nitrocellulose en acrylcoatings. It wurdt brûkt yn ferveferwiderers, lakken, fernissen, spuitferven, sealers, lijmen, magnetyske tapes, printinkten, harsen, rosins, reinigingsoplossingen en foar polymerisaasje. It wurdt fûn yn oare konsuminteprodukten, bygelyks húshâldlike en hobbysementen en houtfillingprodukten. MEK wurdt brûkt by it ûntwaaksen fan smeermiddelen, it ûntfetten fan metalen, by de produksje fan keunstlear, transparant papier en aluminiumfolie, en as in gemyske tuskenstof en katalysator. It is in ekstraksjeoplosmiddel by de ferwurking fan iten en itenyngrediïnten. MEK kin ek brûkt wurde om sjirurgyske en toskedokterapparatuer te sterilisearjen.
Neist de produksje omfetsje miljeuboarnen de útlaatgassen fan jet- en ynterne ferbaarningsmotoren, en yndustriële aktiviteiten lykas fergassing fan stienkoal. It wurdt yn substansjele hoemannichten fûn yn tabaksreek. MEK wurdt biologysk produsearre en is identifisearre as in produkt fan mikrobiële metabolisme. It is ek fûn yn planten, ynsektenferomonen en dierweefsels, en MEK is wierskynlik in lyts produkt fan normale sûchdiermetabolisme. It is stabyl ûnder gewoane omstannichheden, mar kin peroxiden foarmje by langere opslach; dizze kinne eksplosyf wêze.
Produktkategoryen
-

Telefoan
-

E-post
-

Whatsapp
-

Top













